【科研前沿】人体微生物组全解析:结合宏蛋白组学与代谢组学的研究框架
人体内部栖息着数量庞大的微生物群体,这些微生物分布于肠道、皮肤、口腔等不同部位,形成了各自独特的微生物生态系统,而其中以肠道微生物群落最为重要。它们在维护宿主健康方面扮演着不可或缺的角色。️通过运用多组学技术——基因组学、转录组学、蛋白质组学和代谢组学,能够进一步了解微生物群落的构成、功能及其随时间的变化情况。
人体微生物群落与宿主之间存在着复杂的相互作用,这种互动在生理、免疫和代谢等多个层面均有所体现。一方面,微生物群落通过调节宿主的免疫系统,参与抗病防御和免疫耐受的建立,成为宿主健康的重要保障。另一方面,微生物通过生成代谢产物,如短链脂肪酸、氨基酸和维生素等,直接作用于宿主的代谢系统,调控能量平衡,优化营养摄取。更为引人注目的是,微生物还能借助代谢产物或信号分子,通过肠脑轴这一桥梁,影响宿主的神经系统,进而调控情绪和行为。
然而,当微生物群落出现失衡时,它们可能转而成为疾病的诱因。肥胖、糖尿病、炎症性肠病、自身免疫疾病以及神经退行性疾病等多种疾病的发生,均与微生物群的失调紧密相关。通过微生物多组学研究,我们不仅能够揭示这些疾病的潜在发病机理,还能为疾病的早期诊断、预防以及个性化治疗提供新颖的生物标志物和干预靶点。
人体微生物多组学研究不仅加深了我们对微生物与宿主相互关系的理解,还为精准医学、肠道健康管理以及疾病干预策略的制定提供了宝贵的思路。这一领域的研究因此成为历年来科研界的热点,引领着未来健康与医学发展的新方向。
️多组学技术综合分析常见研究思路
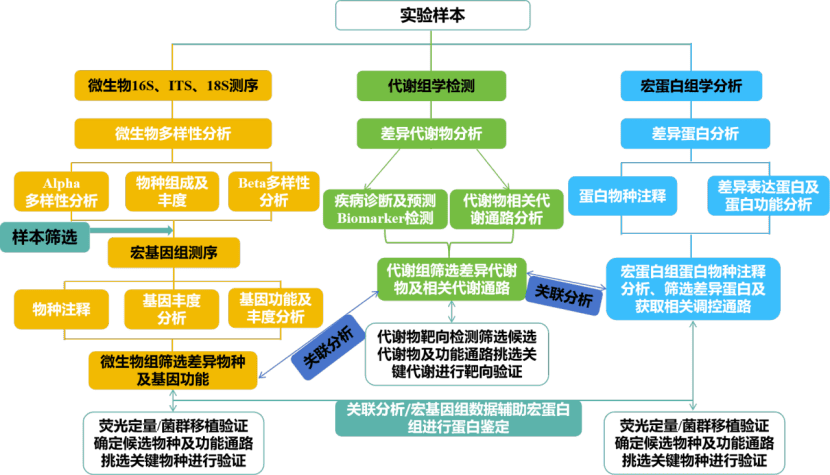
️1、基因功能与代谢通路分析
宏基因组学+代谢组学数据: 获得基因功能注释,解析代谢通路,从而揭示微生物功能基因对代谢的影响。
️2、蛋白质功能与代谢通路分析
宏蛋白质组学+代谢组学,了解微生物产生的蛋白质在代谢反应中的作用,分析微生物如何通过其代谢产物和蛋白质与宿主相互作用。
️3、基因功能与蛋白质功能分析
aspcms.cn用宏基因组数据辅助宏蛋白组进行蛋白鉴定;
基因组维度和蛋白组维度分别获得物种组成,看两个层面的一致性和差异性;
宏蛋白组对宏基因组数据进行补充,完善物种功能。
️4、多组学分析
整合多组学数据,深入探讨微生物群落的动态变化如何与宿主的生理、免疫和代谢反应相互关联,从而影响宿主的健康状态或疾病发展。
️各组学研究意义与主要结果分析
️01 微生物扩增子测序
️研究问题:微生物群落的物种组成和多样性分析
️生物学意义:主要用于鉴定微生物群落中的物种组成。通过分析16S rRNA/ITS/18SrRNA基因的序列,可以识别样本中存在的细菌/真菌/真核生物物种及其相对丰度。
️应用:探索微生物生态学及其与宿主相互作用的重要工具。
️结果展示:
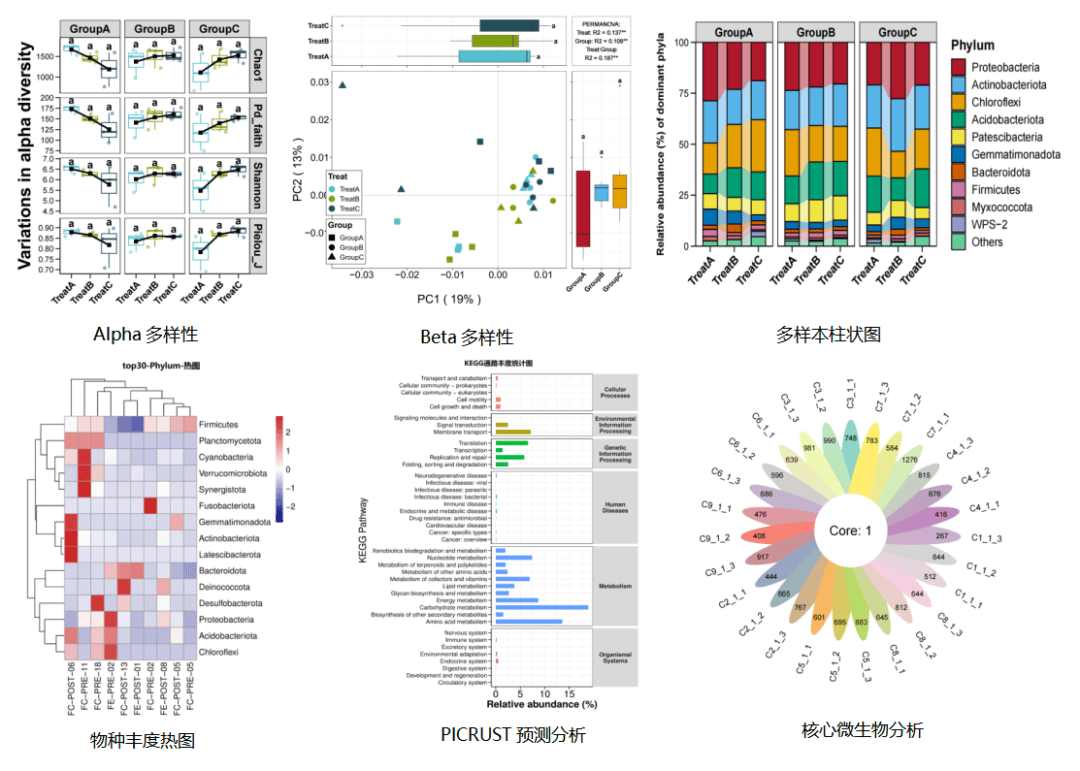
️02 宏基因组
️研究问题:微生物群落的物种分析和基因功能
️生物学意义:在基因组水平解读微生物群体的多样性和丰度,探索微生物与环境及宿主之间的关系。
️应用:能够阐明微生物群在特定生态环境(如肠道、皮肤等)中的关键作用,有助于深入理解微生物对宿主代谢过程、免疫系统功能以及疾病发展的潜在影响。还能揭示与特定疾病(例如肠道菌群失衡、癌症等)相关联的功能基因,进而为预测疾病风险提供有力依据。
️结果展示:
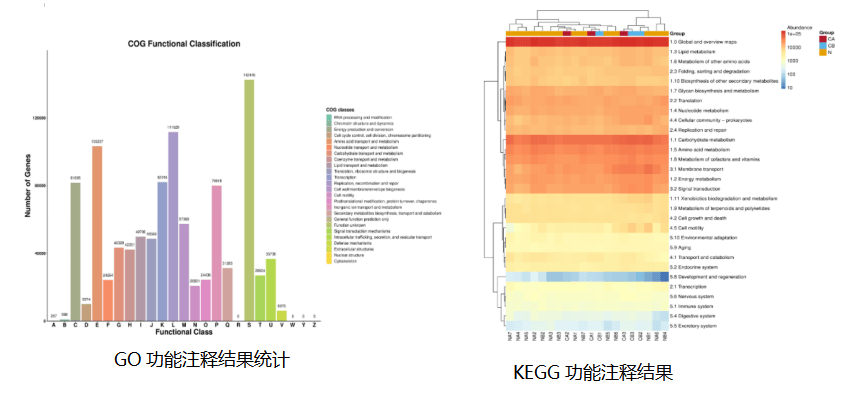
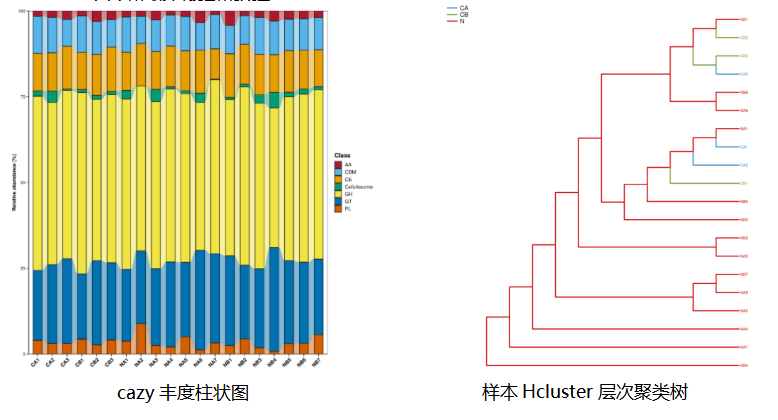
️03 宏蛋白质组学
️研究问题:微生物群落的蛋白质表达功能和动态调控。
️生物学意义:主要关注微生物群落中的蛋白质表达情况,通过质谱分析技术定量和鉴定样本中的所有蛋白质。不同于宏基因组学,宏蛋白质组学直接反映了微生物群体在特定条件下的蛋白质产物,这些蛋白质是微生物的生理功能和代谢活性的关键。
️应用:研究微生物如何在宿主环境中发挥作用,如通过产生酶、毒素或其他功能蛋白来影响宿主的代谢和免疫反应。它可以揭示微生物群落在健康或疾病状态下的生理变化,探索与疾病相关的蛋白质标志物。
️结果展示:
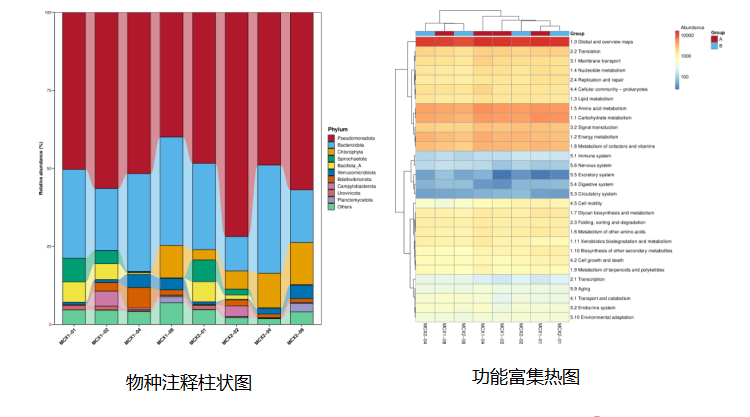
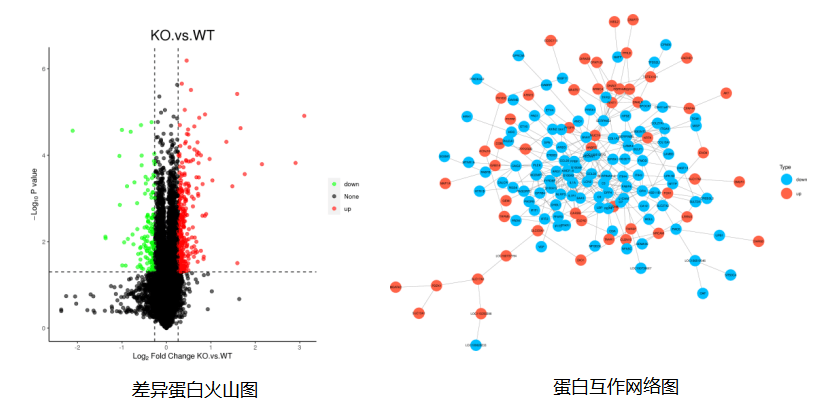
️04 代谢组学
️研究问题:对目标代谢物进行分析及其对宿主的影响。
️生物学意义:对生物体内所有代谢物进行全面的定性和定量分析,研究这些代谢物在不同生理或病理条件下的动态变化规律,从而揭示生物体的代谢状态和生理功能。
️应用:研究微生物代谢途径和代谢物,揭示不同环境下的代谢变化。同时,探索微生物与宿主的相互作用,了解双方的代谢影响。还可以助力筛选疾病标志物,揭示与疾病相关的代谢物群,分析代谢物变化可预测疾病早期发生,研究发病机制。
️结果展示:
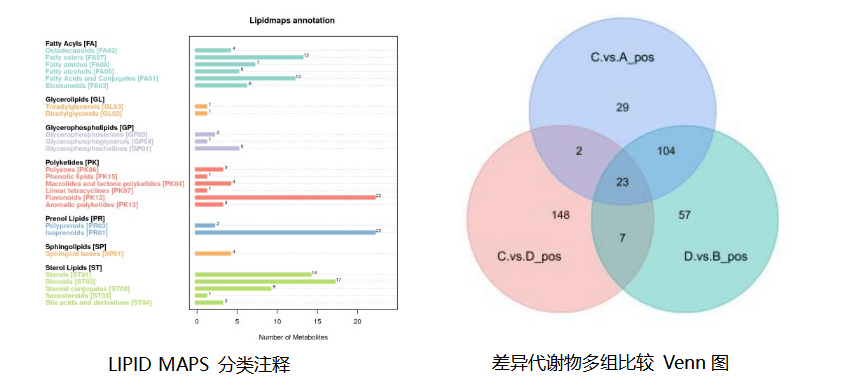
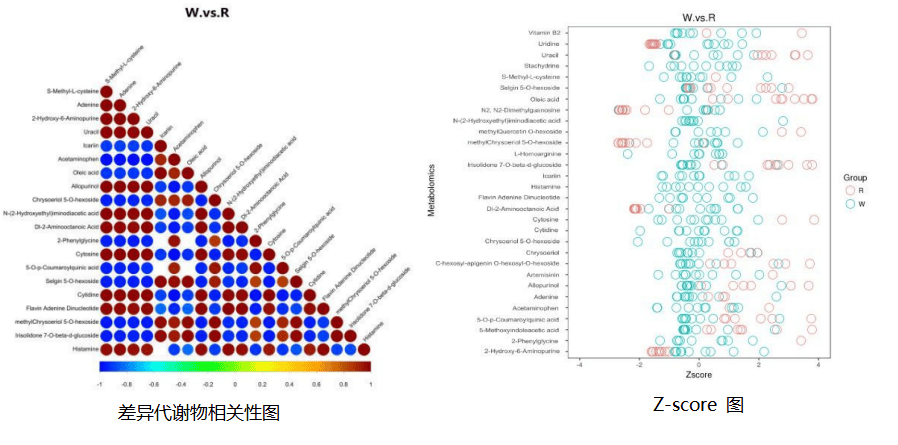
️高分文章案例
️01、粪便微生物转移和复合碳水化合物介导对慢性阻塞性肺病的保护[1]

️发表期刊:Gut
️影响因子:23
️研究策略:宏基因组+蛋白组+代谢组学
️研究背景:慢性阻塞性肺病(COPD)最常由长期吸入香烟烟雾(CS)引起,然而COPD的发病机制复杂,传统治疗方法效果有限,因此,本文研究了慢性阻塞性肺疾病(COPD)的发展机制与肠道微生物之间的关系,并评估了粪便微生物转移(FMT)作为潜在治疗策略的效果,并为开发基于 FMT 的新型治疗方法提供了理论依据。
️研究思路
️• 使用小鼠模型,通过吸入香烟烟雾(CS)诱导COPD。
️• 利用粪菌移植(FMT)技术,将健康小鼠的肠道微生物转移到CS暴露的小鼠中。
️• 通过宏基因组学、16S rRNA、蛋白质组学和代谢组学分析粪便微生物群。
️• 将结果与气道和全身炎症、肺和肠道组织病理学以及肺功能相关联。
️• 在CS暴露小鼠中使用高抗性淀粉饮食评估复合碳水化合物,并在16名COPD人类患者中使用菊粉进行随机、双盲、安慰剂对照试点研究。
️主要结果
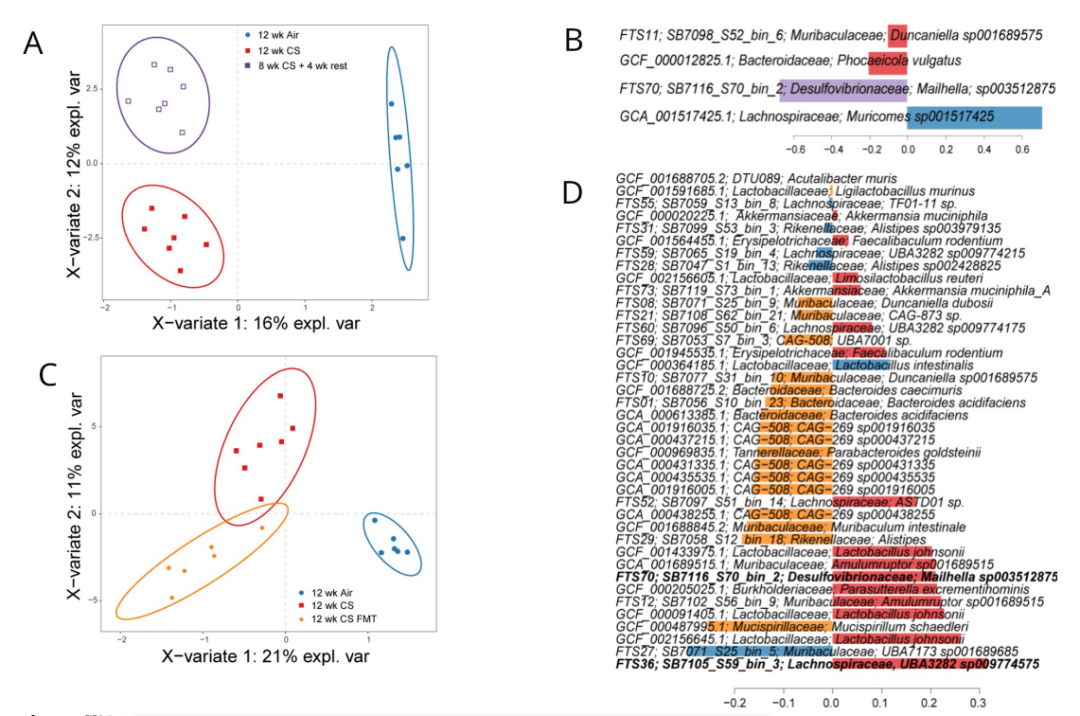

️研究结论
️• FMT缓解了COPD的标志性特征(炎症、肺泡破坏、肺功能受损)、胃肠道病理和全身免疫变化。
️• 疾病特征与Muribaculaceae、Desulfovibrionaceae和Lachnospiraceae家族的相对丰度相关。
️• 宏蛋白质组学和代谢组学鉴定出CS相关微生物群中葡萄糖和淀粉代谢的下调,补充复合碳水化合物可以改善疾病结果。
️• 肠道微生物群参与了COPD的发病机制,可以作为靶向治疗。
️02、UC患者肠道微生物多组学分析揭示普通拟杆菌蛋白酶与疾病严重程度相关[2]

️发表期刊:Nature Microbiology
️影响因子:20.5
️研究策略:宏蛋白质组学+代谢组学+宏基因组学+16S rRNA扩增子
️样本类型:溃疡性结肠炎(UC)患者粪便和血清
研究背景:溃疡性结肠炎(UC)是一种慢性炎症性肠病,与宿主-微生物群稳态失衡相关,其特征是结肠的慢性炎症,目前的治疗方式主要集中在宿主的炎症通路,但对于宿主-微生物群相互作用在UC中如何被破坏尚不清楚。
️研究思路:
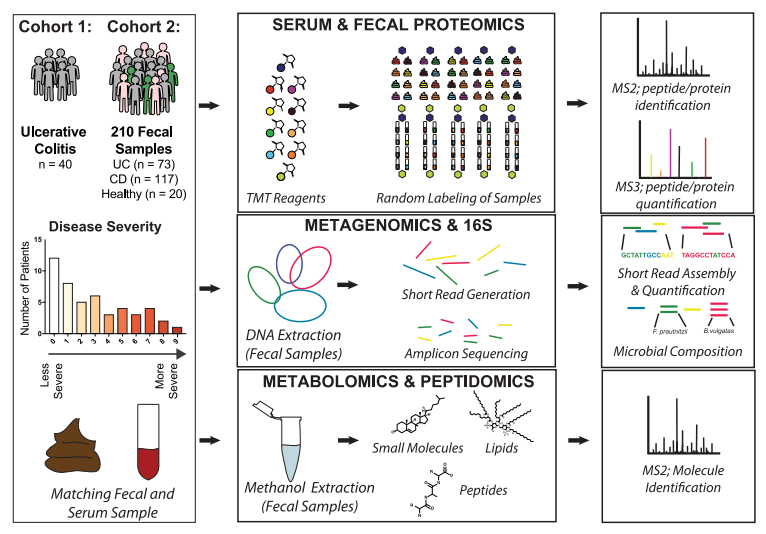
️• 发现队列:40名溃疡性结肠炎(UC)患者的粪便和血清的组学数据集;独立验证队列,210份粪便样本,包括 73例UC患者,117 份克罗恩病(CD)患者,20份炎症性肠病(IBD)患者。
️• 整合两个队列的数据,研究与UC疾病严重性相关的微生物群落的变化情况。
️• 使用Caco-2细胞模型测试UC中六种丰度最高的拟杆菌对肠道屏障的影响,并测试了广谱蛋白酶抑制剂的效果。
️• 结合蛋白组学和代谢组学对粪便和血清样本进行分析,从而识别与UC疾病相关的微生物蛋白质和代谢产物。
️主要结果
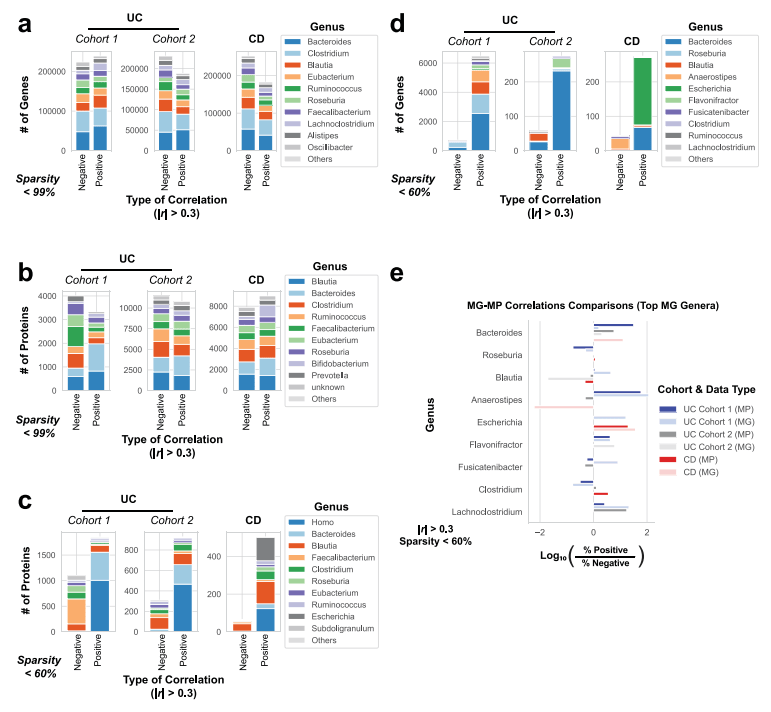
️研究结论:
️• 多组学联合分析发现,肠炎疾病严重程度与α多样性和β多样性均显著相关。另外粪便的组学数据之间的相关性优于血清蛋白质组,粪便宏蛋白质组对UC预测能力最优,其次是多组学联合分析及代谢组。
️• 通过整合多组学数据以及体内外双重验证,证明了微生物组的某些成员,例如B. vulgatus,可能通过蛋白酶活性影响UC疾病严重程度,表明抑制B. vulgatus蛋白酶可能具有治疗或预防UC的作用。
️03、婴儿肠道微生物群有助于小鼠认知表现[3]

️发表期刊:Cell Host & Microbe
️影响因子:20.6
️研究策略:16S rRNA+宏蛋白质组学+靶向代谢组学
️样本类型:婴儿粪便、小鼠粪便
️研究背景:肠道微生物群通过多种途径与大脑交流,影响情绪和行为,这表明了微生物群-肠-脑轴的存在。在人类中,肠道微生物群的组成与儿童早期的行为和情绪问题有关,但具体的作用机制尚不清楚。
️研究思路
️• 通过16S rRNA测序分析了解Inf-aboveCC和Inf-belowCC婴儿肠道菌群的组成和多样性。
️• 宏蛋白质组学分析微生物群的功能特征。
️• 靶向代谢组学检测粪便、尿液和血液中的组氨酸代谢
️• 菌群移植实验,将Inf-aboveCC和Inf-belowCC婴儿的粪菌分别移植到两组小鼠体内,研究不同微生物群对小鼠认知功能的影响。
️主要结果
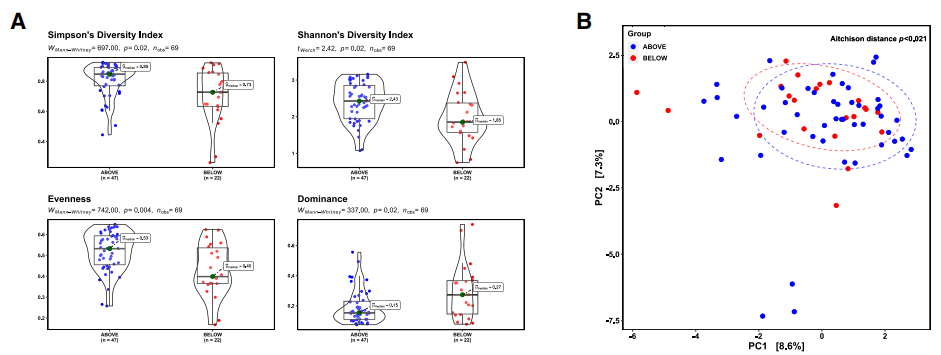
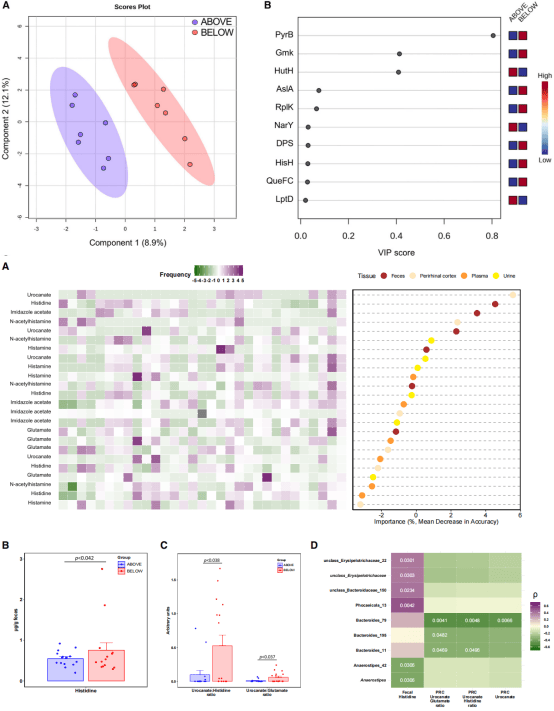
️研究结论
️• 通过16S rRNA测序技术,研究者们发现Inf-aboveCC组的婴儿肠道中Phocaeicola、Bacteroides和Bifidobacterium等细菌的丰度更高,表明认知能力高于中位数的婴儿的肠道微生物群表现出更高的多样性和均匀性。
️• 宏蛋白质组学、靶向代谢组学分析揭示了微生物组氨酸裂氨酶和组氨酸代谢物与认知之间的关联,这表明肠道微生物群可能通过调节组氨酸代谢物水平来影响影响记忆和学习能力。
️• 通过粪便微生物群移植,证实了肠道微生物群对认知的促进特性可以通过粪菌移植传递给小鼠,从而调节与认知功能相关的神经递质和代谢物的可用性,来影响记忆和学习能力。
️参考文献
[1]Faecal microbial transfer and complex carbohydrates mediate protection against COPD [J]. ️Gut. 2024.
[2]Multi-omics analyses of the ulcerative colitis gut microbiome link Bacteroides vulgatus proteases with disease severity. ️Nature Microbiology. 2022.
[3]Infant gut microbiota contributes to cognitive performance in mice. ️Cell Host Microbe. 2023.


