Nature 报道 | 糖尿病患者的福音!基于深度选择性拉曼光谱的高精度无创血糖检测技术
2025年2月5日,️上海交通大学医学院附属瑞金医院王卫庆教授团队、瑞金医院医学芯片研究所及️上海近观科技的️陈昌研究员团队,合作在《Nature Metabolism》发表题为“Subcutaneous depth-selective spectral imaging with mμSORS enables non-invasive glucose monitoring”的研究论文。
️该研究提出了一种新型的非侵入式无创血糖检测系统(mμSORS)。通过在不同的皮肤深度捕捉拉曼信号,检测人类的血糖水平。研究团队还确定了最佳的检测深度,位于皮肤的真皮-表皮交界处或其以下。
️未来,只需要将手放在检测仪器上,就能测量出血糖水平。全程无创、无痛,完美规避以往血糖检测方式的潜在风险。

24年末,《柳叶刀》发表的研究指出,全球糖尿病患者️超8亿人。血糖检测对糖尿病患者至关重要。
近年来,微创连续血糖检测技术虽有进展,但使用不便。️非侵入式无创血糖检测技术是当前研究热点,但现有方法存在准确性不足或需个性化校准的问题。
️拉曼光谱技术因高特异性识别葡萄糖分子而备受关注,但传统拉曼光谱方法受限于实际应用。

本研究开发并验证了一种新型的深度选择性拉曼光谱技术--️多重微空间偏移拉曼光谱(mμSORS, multiple μ-spatially offset Raman spectroscopy),该技术通过更精确的深度控制,能够有效捕捉与血糖相关的拉曼信号,提供更高精度的️非侵入性无创血糖测量。
研究发现,特定的拉曼峰与静脉血浆血糖浓度有强相关性。在包括230名参与者的第二项研究中,研究者优化了回归模型,达到了14.6%的平均绝对相对误差,且99.4%的血糖值落入了临床公认的共识误差网格的临床可接受区域。

️mµSORS检测皮肤层次的深度选择性拉曼信号
与传统的SORS技术相比,mμSORS通过光纤阵列的微米级偏移实现了更高的深度分辨率,在皮肤表层到真皮层之间能够有效区分信号,从而提升了血糖检测的准确性。
通过结合光学相干断层扫描(OCT)技术,mμSORS系统能够根据不同偏移量精确捕捉来自皮肤不同深度的信号,特别是从真皮层的信号,这对于精准测量血糖浓度至关重要。
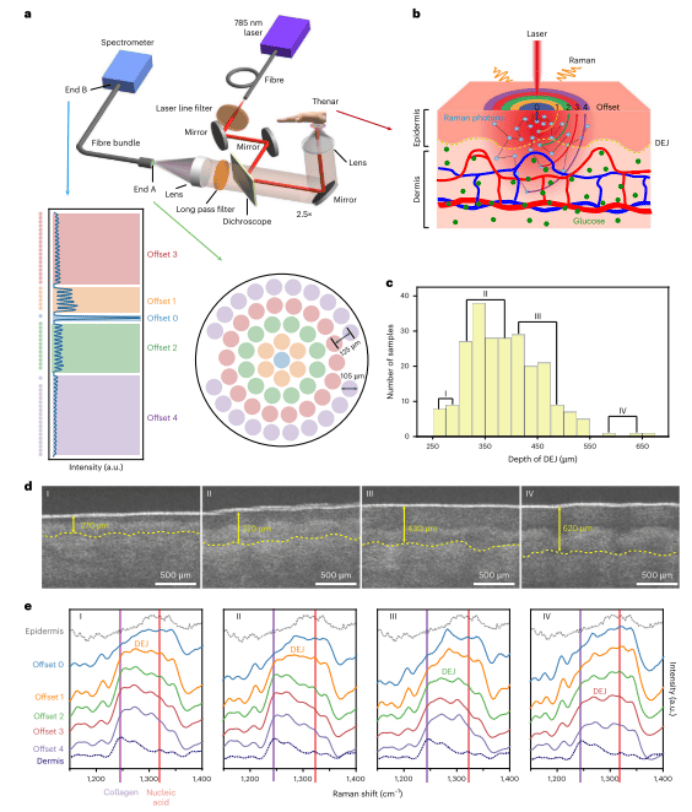
️图1 mµSORS系统可深度选择性地检测从表皮到真皮的拉曼信号。️(a) mµSORS系统的原理图。️(b) mµSORS检测手掌示意图。️(c) 通过OCT识别的来自232个人手掌样本的DEJ深度的直方图。️(d) 从c中标记的I-IV中选择平均DEJ深度为270 μm、370 μm、430 μm和620 μm的四个样本的典型OCT图像。️(e) (d)中相同样品的mµSORS光谱,沿着取自离体人体皮肤表皮和真皮样品的参考拉曼光谱。
️真皮层拉曼光谱与血糖浓度(VPG)高度相关
️相关性: mµSORS能够区分来自皮肤不同深度(如表皮层和真皮层)的拉曼信号。
在初步的BESH实验中,研究发现来自皮肤真皮层的拉曼信号与静脉血浆血糖(VPG)浓度之间呈现出高度的线性相关性。
特别是通过偏移量2-4的光谱,能够捕捉到较深层的信号,与血糖浓度之间保持紧密的线性关系。
因此,可以有效获取与血糖浓度相关的信号,而避免表层信号的干扰。
️优势: 通过分析这些深层的拉曼信号,mμSORS能够有效地识别和预测血糖水平。特别是从真皮层获取的信号,能够有效反映体内血糖水平,并且避免了浅层表皮信号的干扰,提供了更为准确的血糖检测数据。
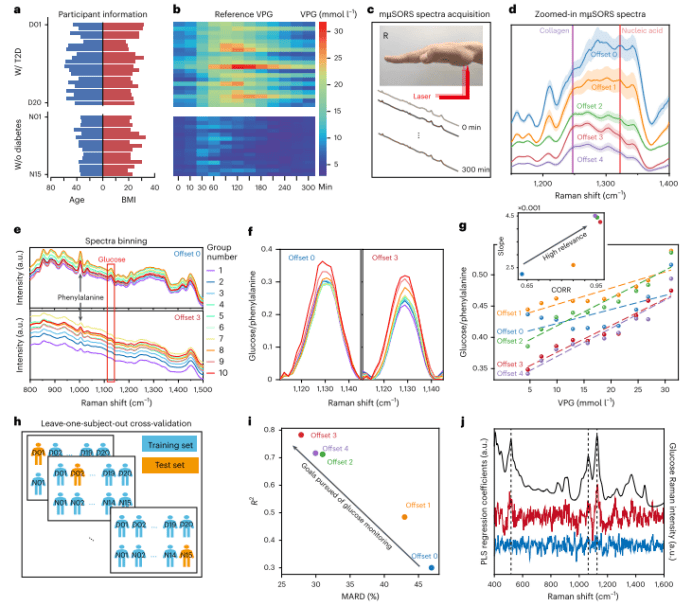
️图2 35例受试者初步BESH中mµSORS光谱与血糖水平的相关性。(️a) 35名受试者的年龄和BMI分布。️(b) 在5小时OGTT期间的12个采样点测量的VPG水平。️(c) OGTT期间mμSORS光谱采集示意图。️(d) 所有参与者在每个偏移处的光谱平均值。️(e) 组号从1到10的10个VPG bin的平均mμSORS光谱。️(f) 用苯丙氨酸条带归一化后葡萄糖峰周围的放大光谱(e中的红色矩形)。️(g) 归一化葡萄糖拉曼谱带(f)对每个偏移量的VPG水平。️(h) PLS模型的留一受试者交叉验证方案示意图。️(i) 在不同偏移量下模型性能的度量。️(j) 从h(浅蓝色,偏移0 ;红色,偏移3)和葡萄糖溶液的拉曼光谱(黑色)获得的平均回归系数。
️准确且个体无关的血糖预测
️高精度预测: 该系统在广泛的血糖水平范围内(包括正常和病理范围)均表现出较高的预测精度,整体平均相对误差(MARD)值低于15%。
通过PLS回归模型,mμSORS能够为不同参与者提供可靠的血糖预测,而无需个体化的设备校准。
️个体无关性: mμSORS在不同参与者之间表现出相似的预测准确性,消除了对个体特征的依赖,使得该系统适用于无个体化校准的临床应用。
这一特性使得mμSORS能够被广泛应用于不同人群,尤其是在没有预先校准的情况下进行血糖检测。
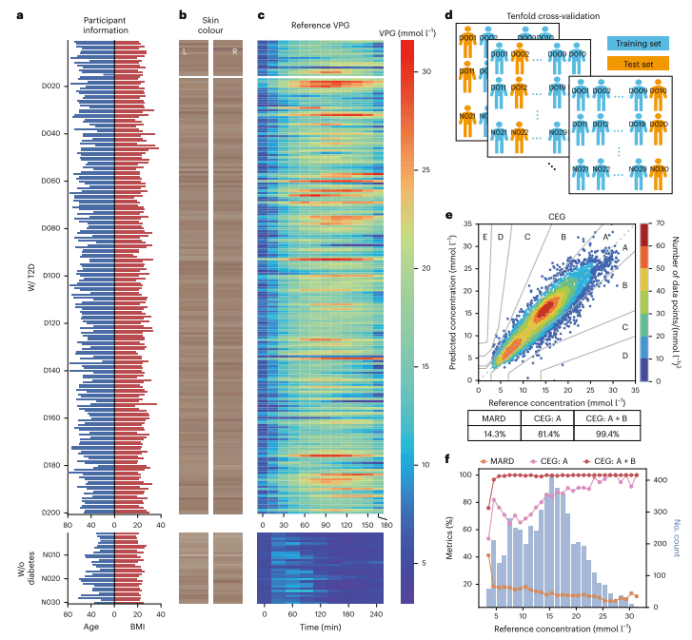
️图3 扩展BESHs中230名参与者的血糖预测,受试者10倍交叉验证。️(a) 230名参与者的年龄和BMI分布。️(b) 230名参与者的皮肤颜色。️(c) OGTT期间测量的230名参与者的VPG水平。️(d) 受试者10倍交叉验证方案的示意图。️(e) 在交叉验证(d)中来自PLS回归模型的预测的CEG。️(f) 根据参考葡萄糖浓度绘制的模型性能指标。
️在独立测试集上的实际血糖检测
️独立测试集验证:在由30名参与者(包括25名2型糖尿病患者和5名健康人群)组成的独立测试集上,mµSORS再次验证了其高精度和临床可行性。
️实验结果表明,99.4%的血糖预测值落入了临床可接受的范围(CEG A + B区),且大多数参与者的平均绝对相对差(MARD)值低于15%。
这一结果证明了mµSORS在实际临床应用中的有效性。
️不同血糖水平下的表现:对于糖尿病患者,系统能够准确反映餐后血糖的单相变化曲线;对于健康个体,系统能够反映血糖的平稳变化,证明其适用于不同血糖水平的参与者。
️预测趋势一致性:对每个参与者,无论使用哪只手,系统的预测结果均显示出良好的精确度,并且预测的血糖浓度与VPG值呈现高度一致。
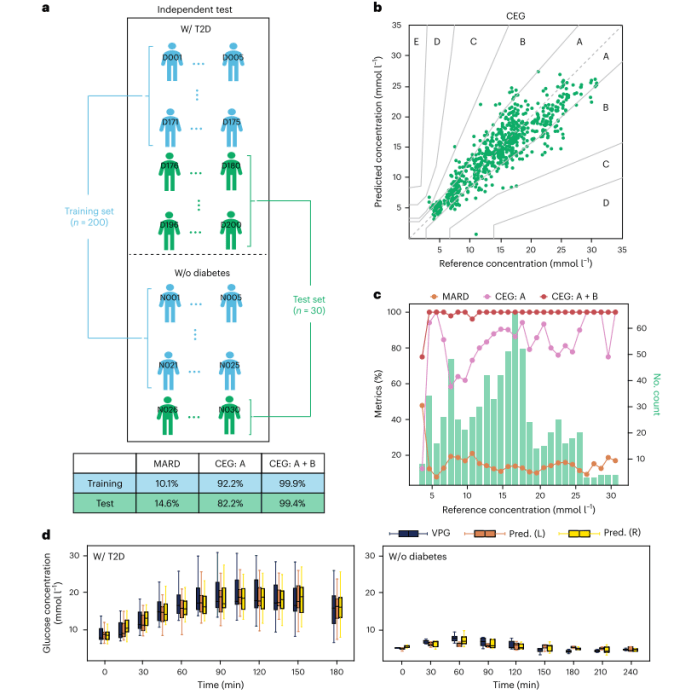
️图4 基于独立测试数据集的血糖预测。️(a) 独立数据集上的模型训练(n = 200)和测试(n = 30)示意图(上图)。️(b) 测试集上来自PLS回归模型的预测的CEG。️(c) 针对测试集中的参考葡萄糖浓度绘制的模型性能指标。️(d) OGTT期间试验组中T2 D参与者和非糖尿病参与者的预测和参考葡萄糖浓度的总体趋势。在箱形图中,箱形边界表示Q1(第25百分位数)和Q3(第75百分位数)。
️局限与展望
mµSORS在技术进步和临床适用性方面取得显著成就,但仍面临一些挑战。
未来,随着技术进步,️mµSORS有望通过集成芯片和可穿戴设备进一步改进。可使用空间外差光谱将拉曼光谱仪集成到芯片级,该空间外差光谱可以在200 mm CMOS兼容硅光子平台中制造。可将mµSORS封装到可穿戴设备中可以扩展其测量人体皮肤上各种部位的能力,使葡萄糖拉曼光谱可以达到更高的信噪比。
(本文来源于Nature,仅作为行业信息和新闻分享)


